المجال
: المادة وتحولاتها
الوحدة : مدخل إلى الكيمياء العضوية
الاستاذ : سعد الله أحمد
عناصر الوحدة :
|
1.
مدخل الى الكيمياء العضوية
2.
الفحوم الهيدروجنية
3.
الكتابة الطوبولوجية للفحوم الهيدروجنية
4.
التسمية حسب توصيات IUPAC للفحوم
الهيدروجينية المشبعة وغير المشبعة
5.
الألكانات
6.
الألكنات
7.
الألكينات
8.
العائلات
9.
الكحولات
10.
الأحماض الكربوكسلية
11.
الأسترات
12.
الألدهيد
13.
الكيتون
14.
الأحماض الأمينية
ثانوية صلاح الين الأيوبي –المسيلة - السنة : ثانية تقني رياضي
المجال : المادة وتحولاتها
الوحدة : مدخل إلى الكيمياء العضوية الاستاذ : سعد الله أحمد
الكفاءات المستهدفة :
- يكون قادرا على تسمية النظامية للمركبات العضوية .
- يتعرف على بعض العائلات العضوية .
- يتعرف على المواد المشتقة من البترول و استعمالاتها في الحياة اليومية ة تأثيرها على المحيط وعلى البيئة .
الـــــــــــــــدرس
مدخل إلى الكيمياء العضوية :
الكيمياء العضوية من الممكن أن تعرف ببساطة بأنها كيمياء مركبات الكربون. وكلمة عضوية Organic
ناشئة من كون المركبات العضوية يمكن الحصول عليها فقط من مصادر نباتية و حيوانية، أي أنها تستمد من
الكائنات الحية.
ودراسة الكيمياء العضوية مهمة جداً في الكثير من المجالات التي تؤثر بشكل مباشر أو غير مباشر في حياة
الإنسان و سعادته. فهي كيمياء المكونات الأساسية للنباتات و الحيوانات، كالبروتينات و الكربوهيدرات
و الفيتامينات و المواد الدهنية والأنزيمات والهرمونات وغيرها، كما أن المركبات العضوية مهمة في صناعة
الملابس التي نلبسها، والوقود الذي نستعمله في المصانع، و لتحريك السيارات و الطائرات و السفن، كما تدخل
في صناعة الورق والمطاط و البلاستيك، والمبيدات الحشرية و الأسمدة، و المتفجرات وغيرها.
و يعد البترول والغاز الطبيعي والفحم من أهم المصادر التي نحصل منها على الكثير من المركبات العضوية
و لتسهيل دراسة هذا العدد الكبير من المركبات العضوية، فقد قسمت تلك المركبات إلى عدد من المجموعات
التي لها تشابه كبير في الخواص الفيزيائية والكيميائية.
النشاط (01) :الفحوم الهيدروجينية _
تعريف الفحوم الهيدروجينية : هي الأنواع الكيميائية العضوية التي تتألف جزيئاتها من عنصر الكربون
و الهيدروجين فقط ، أي هي المركبات العضوية التي صيغتها العامة من الشكل : Cx Hy
السلاسل الفحمية المختلفة للفحوم الهيدروجينية :
الفحوم الهيدروجينية متعددة الكربون تصنف من حيث بنية هيكلها الكربوني إلى صنفين :
الفحوم الهيدروجينية ذات السلاسل المفتوحة :
هي التي تكون فيها ذرات الكربون مرتبطة فيما بينها مشكلة سلسلة مفتوحة ، يمكن لهذه السلسلة أن تكون
خطية أو متفرعة .
مثال :
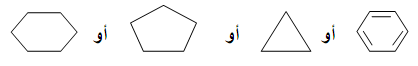
الفحوم الهيدروجينية ذات السلاسل الحلقية : هي التي تكون فيها ذرات الكربون مرتبطة فيما بينها مشكلة حلقة
مثال :
تطبيق : أعط تمثيل سلاسل المركبات التالية : C2H6 ، C3H8
الكتابة الطبولوجية للفحوم الهيدروجينية :
أمثلة :
- الكتابة الطبولوجية للهيكل الكربوني التالي : 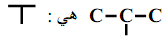
- الكتابة الطبولوجية للهيكل الكربوني التالي : 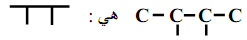
ب- تكافؤ الكتابات الطبولوجية :
كتابات طبولوجية متكافئة بالتشويه : 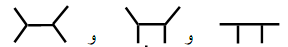
كتابات طبولوجية متكافئة بالتدوير : 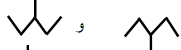
تطبيق : إكمال الجدول :
تعريف : هي المركبات الكيميائية التي لها نفس الصيغة الجزيئية المجملة (نفس عدد الذرات المكونة للجزيئات ).
وبنية جزيئية مختلفة ( صيغتها المنشورة مختلفة ) فهي أنواع كيميائية مختلفة في الخواص الفيزيائية و الكيميائية .
رغم تماثل صيغتها المجملة و توجد عدة أنواع من التماكب .
- المماكب الوضعي : لها نفس السلسلة الرئيسية و الجذور ، ولكنها تختلف في مواضع التفرع ( ذرات الكربون التي ترتبط بالجذور ) .
مثال :
- المماكب التسلسلي : لها نفس الصيغة المجملة و تختلف في شكل سلاسلها .
مثال :
التسمية حسب توصيات IUPAC للفحوم الهيدروجينية المشبعة وغير المشبعة
لللألكانات أسماء مختلفة مركبة من جزئين :
- سابقة من أصل إغريقي تدل على عدد ذرات الكربون التي تحتويها .
- لاحقة ( آن ane ) مشتركة لكل الألكانات للتعبير عن انتمائها لهذه العائلة .
مثال : جدول -1- أسماء لبعض الألكانات
مثال : جدول أسماء بعض الجذور الألكيلية
مثال : أكتب اسم المركب ذي الصيغة المنشورة التالية : CH3-CH-CH2-CH2-CH2-CH3
CH3
2 -مثيل هكسان
* الألسانات (الألكانات) :
أ- الصيغة العامة : هي من الشكل CnH2n حيث هذه الصيغة صحيحة لجزيئات تحتوي على رابطة مزدوجة ، بينما الألسانات التي تحتوي على رابطتين مزدوجتين تكون الصيغة العامة من الشكل CnH2n-2 و الألسانات هي فحوم هيدروجينية غير مشبعة لاحتوائها على روابط مزدوجة و التي تسمى الرابطة غير مشبعة .
تسمية الألسانات وفق IUPAC :
نبدأ بتعيين السلسلة الرئيسية و هي أطول سلسلة تحتوي على رابطة ثنائية و نبدأ الترقيم من الطرف الأقرب لهذه الرابطة .
مثال : CH3-CHCH3-CCH3=CH-CH3 3،4- ثنائي مثيل -2-إن
* الألسينات :
أ - الصيغة العامة : هي من الشكل CnH2n-2 حيث أنها مركبات تحتوي على رابطة ثلاثية ، وجزيئات السلسلة غير المتفرعة تكون ذراتها على استقامة واحدة .
ب – تسمية الألسينات وفق IUPAC : نبدأ بتعيين السلسلة الرئيسية و هي أطول سلسلة تحتوي على رابطة ثلاثية .
و يكتب اسم المركب باعتماد القواعد السابقة مع الإشارة للرابطة الثلاثية باللاحقة ( إين ، yne )
تمرين تطبيقي : أكمل الجدول التالي
* الكحولات : الكحول هو مركب عضوي أكسجيني صيغته العامة من الشكل R-OH . أين R عبارة عن جذر ألكيلي
و (-OH) يسمى في الكيمياء العضوية جذر هيدروكسيل حيث المجموعة الوظيفية ( العائلة ) تكتب بالشكل –CH2OH
و أسماء الكحول مشتقة من الألكانات باستبدال اللاحقة (آن) باللاحقة (ول) . كما تقسم الكحولات إلى ثلاثة أصناف :
كحولات أولية : صيغتها العامة من الشكل R-CH2OH
كحولات ثانوية : صيغتها العمة من الشكل R2-CHOH-R1
كحولات ثالثية : صيغتها العامة من الشكل R1
* الأمينـــــــــــــات :
* الأحماض الكربوكسيلية :
| العودة إلى صفحة الفيزياء التعليم الثانوي |
| صفحة دروس و ملخصات فيزياء السنة ثانوي علمي |
| سلاسل تمارين فيزياء الثانية ثانوي |

